这是一本可以让您快速了解机构,成功完成中心调研的一本手册;
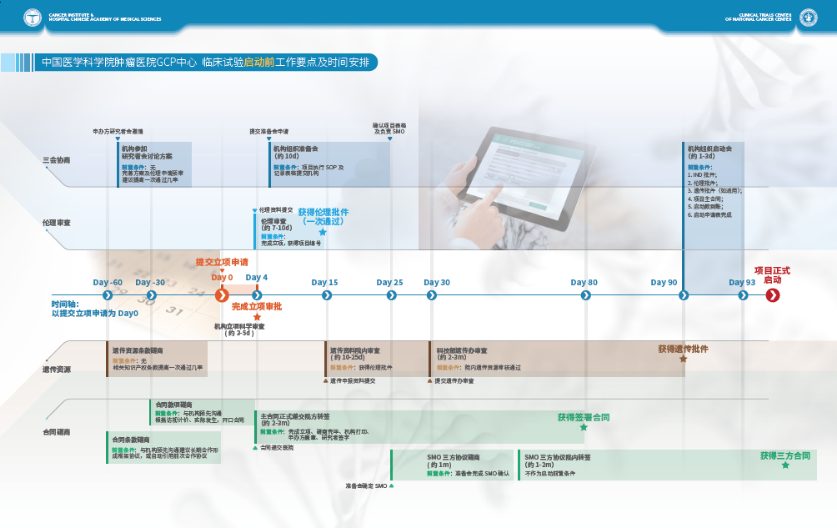
这是一本可以让您快速了解各个环节,成功完成启动前工作的一本手册;
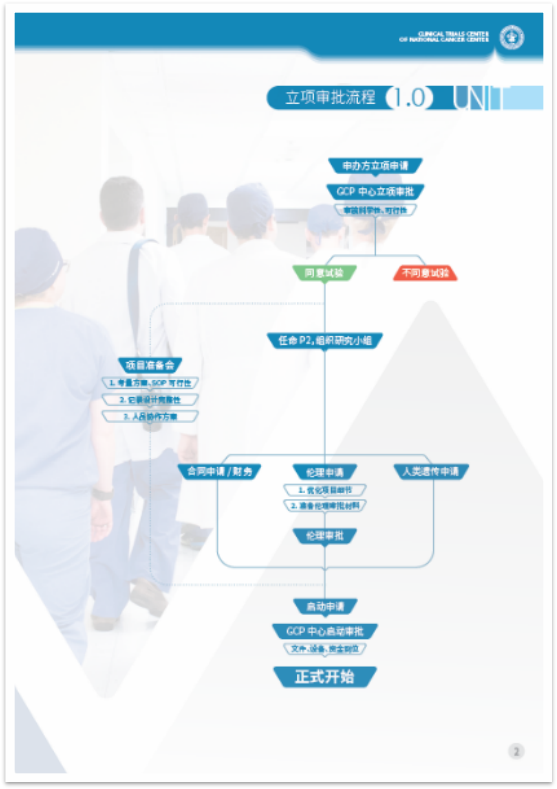
这是一本可以让您快速了解从项目立项、启动到关中心全流程化服务的一本手册。
2017年,中国医学科学院肿瘤医院药物临床试验研究中心(GCP)基于微信公众号陆续发布中心办事指南。
2019年我们将微信公众号办事指南内容装订成册,以1.0版《中国医学科学院肿瘤医院GCP中心办事手册》形式正式发布,内容包括职责分工、伦理、财务、合同、遗传资源、质控、药物、文档管理和SMO入驻等19个模块。
时隔两年,我们基于客户需求再次进行创新整合,在2021年发布的2.0版《办事手册》中:
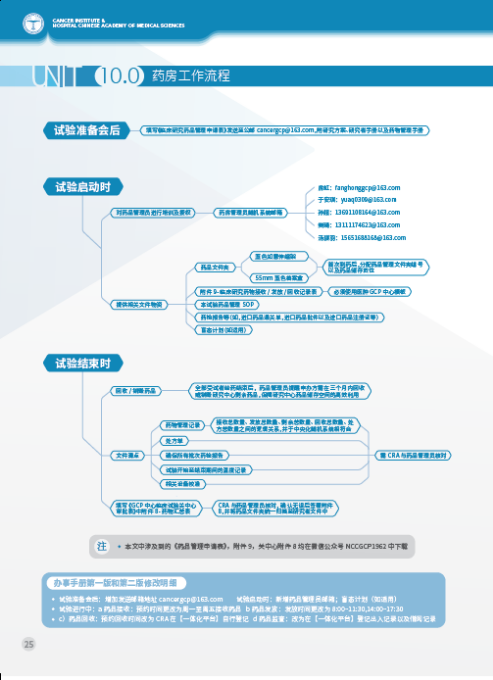
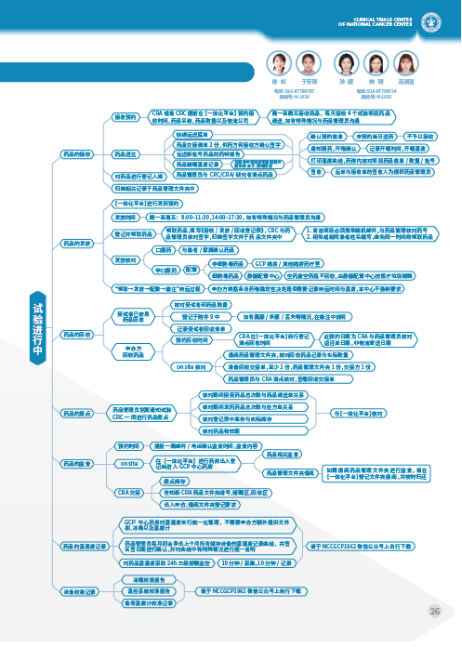
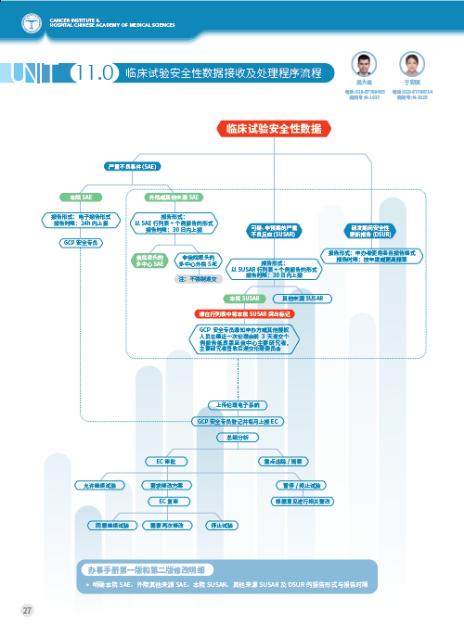
内容上新增:研究中心(SITE)初次沟通与基础情况调研SSU流程,接受申办方/CRO进行中心筛选阶段的研究中心可行性调研以及初次沟通的洽谈工作。研究者发起研究审批流程,为研究者提供更清晰透明的操作流程。研究者会人员邀请流程,前期召开研究者会/方案讨论会优化方案关键环节,为后续顺利开展合作和具体实施提供前期基础。进修实习/参观学习申请流程,GCP中心常年面向临床试验从业人员招收进修实习参观学习人员,培训涵盖GCP知识,机构、伦理工作流程,临床试验病房、门诊管理等内容。
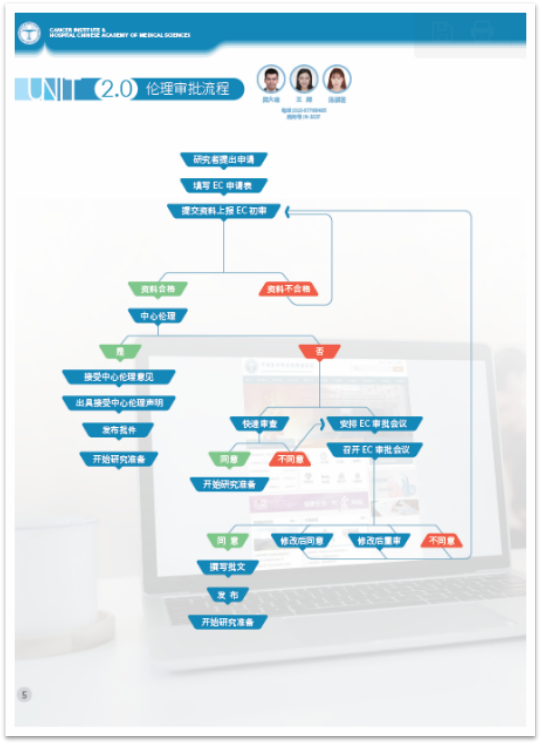
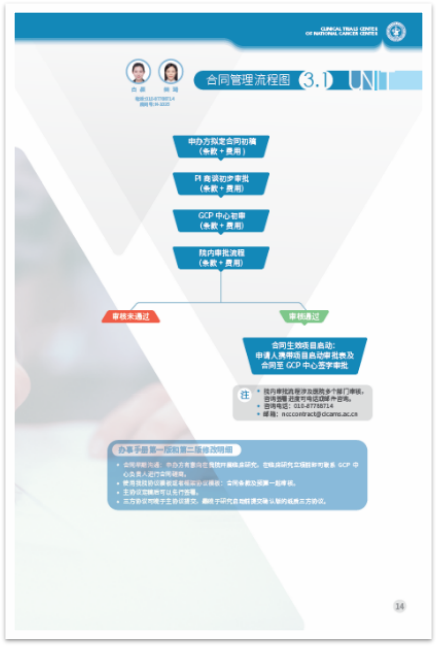
流程上改革:合同早期沟通,申办方有意在我院开展临床研究,在临床研究立项前可进行合同磋商。准备会前置,可在伦理会前召开,加速申办方/CRO时间成本。伦理审查实行全面电子化,真正实现从资料递交、伦理审查、备案、审批结果传达一站式电子化服务等等等等……
2021年即将到来,GCP中心全体工作人员祝您新年快乐,我们诚挚地为您送上新年礼物2021年2.0版《中国医学科学院肿瘤医院GCP中心办事手册》,希望从实操层面为临床试验的一线实践人员提供更便捷的服务,能对您的工作有所帮助,感谢您多年来的支持。
请于文末获取电子版下载链接。










































附件:医科院肿瘤医院GCP中心2021年办事手册.pdf

 010-64929757
010-64929757  service@gcpunion.org
service@gcpunion.org  北京市北三环中路朝阳区安外小关北里43号渔阳置业大厦A座706
北京市北三环中路朝阳区安外小关北里43号渔阳置业大厦A座706 
